What’s new
2026年5月11日(月)「関連試験情報」に「アムベルビスト®︎の注入圧試験結果」を追加しました。
2026年5月11日(月)「動画ライブラリ」に「低用量Gd造影剤アムベルビスト®︎ 製品のご紹介」を追加しました。
2026年3月24日(火) 製品ページを公開しました。
「警告・禁忌を含む注意事項等情報」等は電子添文をご参照ください。
1.警告
1.1
本剤を髄腔内に投与すると重篤な副作用を発現するおそれがあるので、髄腔内には投与しないこと。[14.1.1参照]
1.2
重篤な腎障害のある患者では、ガドリニウム造影剤による腎性全身性線維症の発現のリスクが上昇することが報告されているので、腎障害のある患者又は腎機能が低下しているおそれのある患者では、十分留意すること。[9.2.1-9.2.3、 11.1.2参照]
2.禁忌(次の患者には投与しないこと)
本剤の成分又はガドリニウム造影剤に対し過敏症の既往歴のある患者
開発の経緯
細胞外液性Gd造影剤は、様々な適応症や患者集団を対象に幅広く使用され、臨床的な有用性はすでに評価されています。
そのうち、現在臨床で使用される環状型Gd造影剤は、類似した安全性プロファイルを有しており、Gdキレート安定性が高く、線状型Gd造影剤(現在、国内では販売されていない)と比べて相対的に腎性全身性線維症(NSF)の報告が少ないことが知られています。1,2)
しかしながら、環状型Gd造影剤の場合においても、腎性全身性線維症(NSF)の発症や脳内等のGd残存による潜在的リスク1,2)は、完全には排除されてないと考えております。
また、造影剤に関するガイドライン等では、NSF発症の潜在的リスク軽減の観点から、常に診断に必要な最小限の用量を使用することが推奨されており、Gdへの曝露を低減させるというメディカルニーズが高まっていると認識しております。
そこで、その潜在的リスク軽減のため、既存のGd造影剤と同程度の診断能を担保しながらGd含有量を低減した低用量Gd造影剤(アムベルビスト)の開発が進められました。
Gd造影剤の潜在的リスク1,2)
①腎性全身性線維症(NSF)の発症
- Gd造影剤の重度腎障害患者への投与は、重篤な疾患であるNSFの発症リスクである
- Gd3+の遊離のしやすさがリスク要因の1つであることが示唆されている
②脳内等のGd残存
- 造影MRI検査を複数回受けた患者で、非造影MRI画像上での脳の高信号化や脳の剖検組織からのGdの検出が報告されている
造影剤に関するガイドライン等
- ACR Manual on Contrast Media, 20251)
- ESUR Guidelines 20252)
- EMA’s final opinion, 20173)
- gadolinium-wise MRI—practice recommendations by ESMRMB4)
1)
ACR Committee on Drugs and Contrast Media. ACR Manual on Contrast Media, p70,75-84, American College of Radiology, 2025
(https://edge.sitecorecloud.io/americancoldf5f-acrorgf92a-productioncb02-3650/media/ACR/Files/Clinical/Contrast-Manual/ACR-Manual-on-Contrast-Media.pdf:2026年3月アクセス)
2)
Contrast Media Safety Committee. ESUR Guidedlnes 2025, p24-26,29, European Society of Urogenital Radiology, 2025
(https://www.esur.org/wp-content/uploads/2025/12/Guidelines-2025-ESUR-vf-1.pdf:2026年3月アクセス)
3)
EMA’s Pharmacovigilance Risk Assessment Committee(PRAC). PRAC confirms restrictions on the use of dlnear gadodlnium agent, European Medicines Agency, 2017(www.ema.europa.eu/en/documents/referral/gadolinium-article-31-referral-prac-confirms-restrictions-use-linear-gadolinium-agents_en.pdf:2026年3月アクセス)
4)
Quattrocchi CC, et al.: Eur Radiol. 2025; 35(6): 3347-3353
特性
既存の細胞外液性Gd造影剤※に対して、低いGd用量〔0.04mmol Gd/kg(Gd量を60%低減)〕で有効性(造影効果、辺縁明瞭度、内部構造)における非劣性が検証されました〔国際共同第Ⅲ相試験:QUANTI CNS/OBR試験、主要評価項目(検証的解析結果)〕。
バイエル薬品社内資料[国際共同第Ⅲ相試験:QUANTI CNS試験(試験番号21181)](承認時評価資料)、
バイエル薬品社内資料[国際共同第Ⅲ相試験:QUANTI OBR試験(試験番号21197)](承認時評価資料)1分子中に4つの環状型非イオン性Gdキレートを有する四量体構造で、ガドブトロールよりも高い緩和度を示しました(in vitro 試験)。
バイエル薬品社内資料[効力を裏付ける試験:In vitroにおける緩和時間短縮作用](承認時評価資料)
Gdキレート安定性が高い環状型の非イオン性MRI用造影剤です。
アムベルビスト電子添文(19.有効成分に関する理化学的知見)
血液に近い浸透圧を示す製剤です。
アムベルビスト電子添文(3.2. 製剤の性状)
- 重大な副作用としてショック、アナフィラキシー(いずれも頻度不明)、腎性全身性線維症(頻度不明)があらわれることがあります。主な副作用は、浮動性めまい、頭痛、注射部位反応(いずれも1%未満)でした。
詳細については、電子添文の副作用及び臨床成績の安全性の結果をご参照ください。
効能又は効果
磁気共鳴コンピューター断層撮影における脳・脊髄造影、躯幹部・四肢造影
効能又は効果に関連する注意
ガドリニウム造影剤を複数回投与した患者において、非造影T1強調MR画像上、小脳歯状核、淡蒼球等に高信号が認められたとの報告や脳の剖検組織からガドリニウムが検出されたとの報告があるので、ガドリニウム造影剤を用いた検査の必要性を慎重に判断すること。
用法及び用量
通常、成人及び小児には、本剤0.1mL/kgを静脈内投与する。
体重別用量換算表と該当バイアル/シリンジ
表は横スクロールでご覧いただけます。
| 体重(kg) | 用量(mL) | 該当バイアル/シリンジ |
|---|---|---|
| 5 | 0.5 | バイアル2mL |
| 10 | 1.0 | |
| 15 | 1.5 | |
| 20 | 2.0 | |
| 25 | 2.5 | シリンジ5mL |
| 30 | 3.0 | |
| 35 | 3.5 | |
| 40 | 4.0 | |
| 45 | 4.5 | |
| 50 | 5.0 |
| 体重(kg) | 用量(mL) | 該当バイアル/シリンジ | |
|---|---|---|---|
| 55 | 5.5 | シリンジ7.5mL | |
| 60 | 6.0 | ||
| 65 | 6.5 | ||
| 70 | 7.0 | ||
| 75 | 7.5 | ||
| 80 | 8.0 | シリンジ10mL | |
| 85 | 8.5 | ||
| 90 | 9.0 | ||
| 95 | 9.5 | ||
| 100 | 10.0 | ||
アムベルビスト®︎の薬効・薬理に関する情報
アムベルビストは常磁性のGd3+を含む環状構造の非イオン性ガドリニウムキレート4分子を有する四量体であり、水素原子核の緩和時間を短縮させることにより、磁気共鳴画像の信号強度を上昇させます。
MRI造影剤の緩和度に影響を及ぼす(内的)要因1,2)
- ①不対電子数
- ②配位水数(q)
- ③配位水の交換速度
- ④回転相関時間(キレート錯体の回転運動の速さの目安)
- ⑤金属イオンとプロトンの距離
- ⑥電子スピンの緩和時間 など
キレート構造と回転運動のイメージ図
ガドブトロール
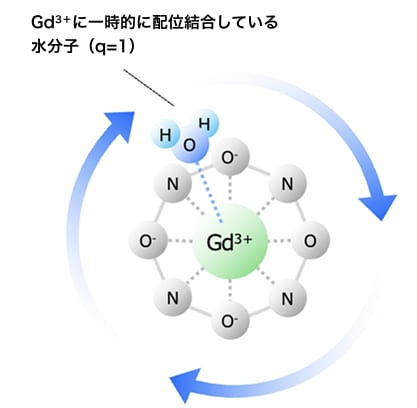
既存のGdキレート錯体は、高速で回転運動しており(GHz)、その回転運動により変動磁場が生じ、水分子のプロトン緩和を誘発する。
この変動磁場の周波数がラーモア周波数(臨床MRIでは20~130MHz)に近い場合、緩和効率は最大化するが、既存のGdキレート錯体はラーモア周波数との乖離が大きいため、緩和効率は制限される3) 。
ガドクアトラン
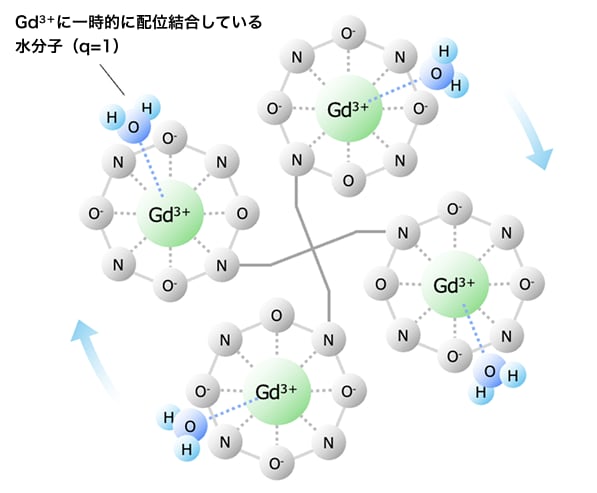
分子量の増大により回転運動が遅くなると、変動磁場の周波数がラーモア周波数に近づくため、緩和度(r1)が高くなる3)。
1)日本磁気共鳴医学会編: NMR医学ー基礎と臨床, 丸善株式会社, 1991
2)笛吹修治: 日獨医報. 2016; 61(1): 119-126
3)Jacques V, et al.: Invest Radiol. 2010; 45(10): 613–624
組成・性状
表は横スクロールでご覧いただけます。
| 販売名 | アムベルビスト静注 2mL | アムベルビスト静注 シリンジ5mL | アムベルビスト静注 シリンジ7.5mL | アムベルビスト静注 シリンジ10mL |
|---|---|---|---|---|
| 有効成分 | 1mL中ガドクアトラン水和物(無水物として)257.9mg含有 | |||
| 1バイアル又は 1シリンジ中の 成分量 | 515.8mg | 1289.5mg | 1934.3mg | 2579.0mg |
| 添加剤 | 1mL中 | |||
| 色・性状 | 無色〜微黄色透明の注射液 | |||
| pH | 6.9〜7.9 | |||
| 浸透圧比 | 約1(生理食塩液に対する比) | |||



