国際共同第Ⅲ相試験
QUANTI CNS試験(海外データ、日本人データを含む)
<脳・脊髄造影における有効性>1)
1)バイエル薬品社内資料[国際共同第Ⅲ相試験:QUANTI CNS試験(試験番号21181)](承認時評価資料)
試験概要
| 目的 | CNS病変を有する又は疑われる成人患者における、アムベルビスト(0.04mmol Gd/kg)の既承認mGBCA(0.1mmol Gd/kg;対照薬は試験方法を参照)に対する非劣性を検証する。 |
|---|---|
| 試験デザイン | 多施設共同、無作為化、二重盲検、クロスオーバー、15ヵ国(アジア、欧州、北米、南米)71施設 |
| 対象 | CNS病変を有する又は疑われる成人患者 |
| 例数(解析時) | 拡大FAS:276例、SAF:303例 〔うち日本人32例(アムベルビスト投与:31例、mGBCA投与:32例)〕 |
| 試験方法 | 各被験者をアムベルビスト(0.04mmol Gd/kg)又はmGBCA(ガドブトロール、ガドテル酸メグルミン又はガドテリドール:各0.1mmol Gd/kg)のいずれかに1:1の割合で無作為割付けし、2つの投与期にアムベルビスト又はmGBCAをクロスオーバーで単回静脈内投与した。1回目と2回目の造影MRI検査の間には3~14日間の休薬期間を設けた。各造影剤の投与前後にMRIを撮像し、非造影画像及び造影画像を取得した。得られた画像を盲検化した状態で独立した3名の読影医及び治験責任(分担)医師により評価した。評価は、MRI検査来院日(投与前から投与後6~8時間)に行った。 
|
| 主要評価項目 | 段階的スコアによる3つの描出パラメータ(造影効果、辺縁明瞭度、内部構造)[アムベルビスト組合せ※3のmGBCA組合せ※3に対する非劣性](検証的解析項目) ![段階的スコアによる3つの描出パラメータ(造影効果、辺縁明瞭度、内部構造)[アムベルビスト組合せ※4のmGBCA組合せ※4に対する非劣性]](/sites/g/files/vrxlpx8716/files/2026-03/products-ambelvist-clinical-trial_img-02.png)
|
| 主な 副次評価項目 | 病変検出能の感度及び特異度[アムベルビスト組合せ※3のmGBCA組合せ※3に対する非劣性] |
| 副次評価項目 | 段階的スコアによる3つの描出パラメータ(造影効果、辺縁明瞭度、内部構造)[アムベルビスト組合せ※3の非造影画像に対する優越性] など |
| 安全性評価項目 | 有害事象、理学的検査(視診、触診及び聴診)、バイタルサイン、臨床検査 |
| 解析計画 |
|
CNS(Central nervous system):中枢神経系
mGBCA(Macrocyclic gadolinium-based contrast agent):環状型Gd造影剤
cSoT(Composite standard of truth):複合的な真の基準
TEAE(Treatment-emergent adverse event):治験薬投与下で発現した有害事象
◆
拡大FAS(Full analysis set):拡大した最大の解析対象集団(「盲検読影に適した造影MRI/MRA画像セットがある」「アムベルビスト組合せ及びmGBCA組合せの両方が評価可能である」の両方を満たすすべての無作為割付けされた被験者)
◆
SAF(Safety analysis set):安全性解析対象集団(アムベルビスト又はmGBCAを投与されたすべての無作為割付けされた被験者)
※ 1
標的臓器の造影MRI検査の照会のために施設の標準治療方針に従って撮像した。
※ 2
施設の標準治療方針に従い、投与期1・2を通じて可能な限り同一条件(タイミング)で撮像した。
※ 3
アムベルビスト組合せ:アムベルビスト(0.04mmol Gd/kg)投与前後の組合せ画像、mGBCA組合せ:mGBCA(0.1mmol Gd/kg)投与前後の組合せ画像
※ 4
安全性の結果では、治験薬と関連のあるTEAEを「副作用」と表記した。
段階的スコアによる3つの描出パラメータ(造影効果、辺縁明瞭度、内部構造)
[アムベルビスト組合せのmGBCA組合せに対する非劣性]【主要評価項目(検証的解析結果)】
3つの描出パラメータにおけるアムベルビスト組合せとmGBCA組合せのスコアの差(最小二乗平均値)は、造影効果で0.09~0.13、辺縁明瞭度で0.01~0.07、内部構造で0.02~0.04でした。3名の読影医において、3つの描出パラメータはいずれもスコアの差の95%信頼区間の上限値が非劣性マージンである0.35を下回り、アムベルビスト組合せのmGBCA組合せに対する非劣性が検証されました。
アムベルビスト組合せ及びmGBCA組合せにおける3つの描出パラメータ(造影効果、辺縁明瞭度、内部構造)のスコア※(拡大FAS)
表は横スクロールでご覧いただけます。
| アムベルビスト組合せ(N=276) | mGBCA組合せ(N=276) | ||
|---|---|---|---|
| 読影医1 | 造影効果 | 2.33±0.066 | 2.45±0.066 |
| 辺縁明瞭度 | 3.34±0.037 | 3.41±0.037 | |
| 内部構造 | 2.68±0.028 | 2.71±0.028 | |
| 読影医2 | 造影効果 | 2.59±0.066 | 2.72±0.066 |
| 辺縁明瞭度 | 3.63±0.037 | 3.68±0.037 | |
| 内部構造 | 2.87±0.028 | 2.91±0.028 | |
| 読影医3 | 造影効果 | 2.15±0.066 | 2.24±0.066 |
| 辺縁明瞭度 | 2.17±0.037 | 2.18±0.037 | |
| 内部構造 | 1.68±0.028 | 1.70±0.028 | |
最小二乗平均値±標準誤差
※
造影効果及び辺縁明瞭度は4段階、内部構造は3段階で評価した。3つの描出パラメータのスコアを線形混合効果モデルにより解析し、アムベルビスト組合せ及びmGBCA組合せの最小二乗平均値及び標準誤差を推定した。
アムベルビスト組合せ及びmGBCA組合せにおける3つの描出パラメータ(造影効果、辺縁明瞭度、内部構造)のスコアの差(拡大FAS)
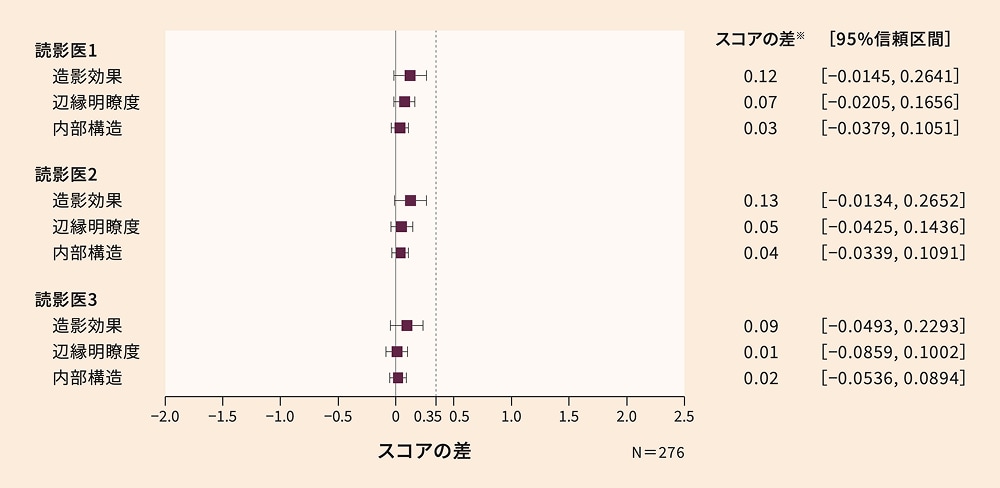
※
mGBCA組合せーアムベルビスト組合せ。3つの描出パラメータのスコアを線形混合効果モデルにより解析した。アムベルビスト組合せ及びmGBCA組合せの最小二乗平均値を推定し、更に各投与群間のスコアの差及びその95%信頼区間を推定した。3名の読影医のうち同じ2名の評価において、アムベルビスト組合せとmGBCA組合せのスコアの差の95%信頼区間の上限値が非劣性マージンである0.35を下回る場合、アムベルビスト組合せのmGBCA組合せに対する非劣性が検証されるものとした。
病変検出能の感度及び特異度[アムベルビスト組合せのmGBCA組合せに対する非劣性]【主な副次評価項目】
アムベルビスト組合せとmGBCA組合せの感度の差の95%信頼区間の上限値は、読影医1で1.54%、読影医2で4.56%、読影医3で1.54%であり、いずれも非劣性マージンである0.1(10%)を下回り、アムベルビスト組合せのmGBCA組合せに対する非劣性が示されました。アムベルビスト組合せとmGBCA組合せの特異度の差の95%信頼区間の上限値は、読影医1で6.40%、読影医2で5.14%、読影医3で17.19%であり、3名の読影医のうち2名において、非劣性マージンである0.1(10%)を下回り、アムベルビスト組合せのmGBCA組合せに対する非劣性が示されました。
アムベルビスト組合せ及びmGBCA組合せにおける病変検出能の感度※1及び特異度※2(拡大FAS)
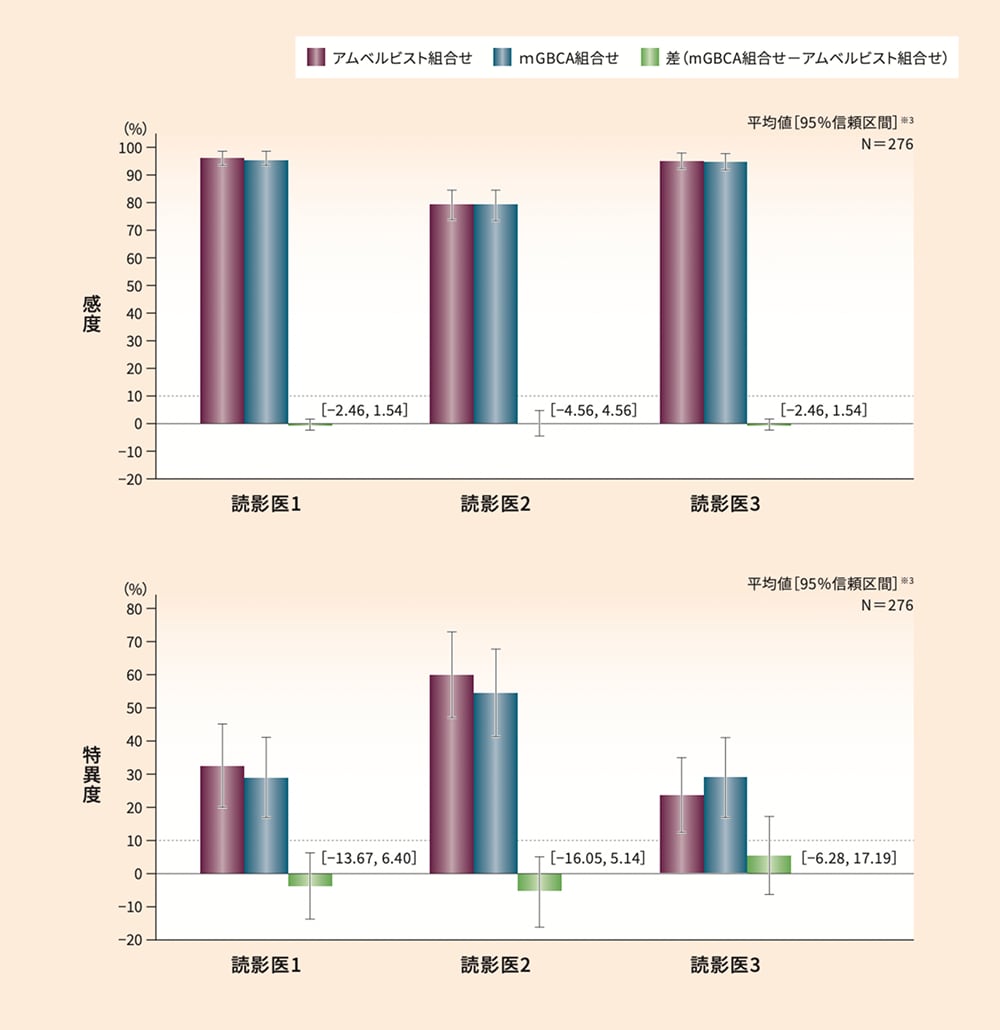
※ 1
読影医によって病変を有すると判定された被験者数をcSoTでの病変を有する被験者の総数で割った値として算出した。
※ 2
読影医によって病変がないと判定された被験者数をcSoTでの病変がない被験者の総数で割った値として算出した。
※ 3
読影医ごとに割合の差についてMcNemar検定に基づく95%信頼区間を算出した。3名の読影医のうち同じ2名の評価において、その上限値が非劣性マージンである0.1(10%)を下回る場合、アムベルビスト組合せのmGBCA組合せに対する非劣性が示されるものとした。
段階的スコアによる3つの描出パラメータ(造影効果、辺縁明瞭度、内部構造)[アムベルビスト組合せの非造影画像に対する優越性]【副次評価項目】
3名の読影医において、3つの描出パラメータのスコアの差(最小二乗平均値)※1は0.22~1.64であり、いずれも統計学的に有意であったため〔p<0.0001(線形混合効果モデル、名目上のp値)〕、アムベルビスト組合せの非造影画像に対する優越性が示されました※2。
※1
アムベルビスト組合せ-非造影画像。造影効果及び辺縁明瞭度は4段階、内部構造は3段階で評価した。3つの描出パラメータのスコアを線形混合効果モデルにより解析した。アムベルビスト組合せ及び非造影画像の最小二乗平均値を推定し、更に各投与群間のスコアの差及びその95%信頼区間並びに標準誤差を推定した。
※ 2
3名の読影医のうち同じ2名の評価において、アムベルビスト組合せと非造影画像のスコアの差が0より大きく、統計学的に有意(片側有意水準:0.025)であった場合、アムベルビスト組合せの非造影画像に対する優越性が示されるものとした。
アムベルビスト組合せ及び非造影画像における3つの描出パラメータ(造影効果、辺縁明瞭度、内部構造)のスコアの差(拡大FAS)
表は横スクロールでご覧いただけます。
| スコアの差 | |||
|---|---|---|---|
| 読影医1(N=276) | 読影医2(N=276) | 読影医3(N=276) | |
| 造影効果 | 1.36±0.061 | 1.64±0.061 | 1.17±0.061 |
| 辺縁明瞭度 | 1.08±0.045 | 1.14±0.045 | 0.22±0.045 |
| 内部構造 | 0.94±0.042 | 0.72±0.042 | 0.36±0.042 |
最小二乗平均値±標準誤差
安全性(SAF)
副作用は、アムベルビスト群では299例中15例(5.0%)に発現し、主な症状として浮動性めまいが5例(1.7%)、熱感が3例(1.0%)、頭痛、そう痒症、錯感覚が各2例(0.7%)に認められました。mGBCA群では299例中17例(5.7%)に発現し、主な症状として浮動性めまいが4例(1.3%)、熱感が2例(0.7%)に認められました。本試験において、重篤な副作用、投与中止に至った副作用、死亡例は認められませんでした。
MedDRA version 27.1
QUANTI OBR試験(海外データ、日本人データを含む)
<躯幹部・四肢造影における有効性>2)
2)バイエル薬品社内資料[国際共同第Ⅲ相試験:QUANTI OBR試験(試験番号21197)](承認時評価資料)
試験概要
| 目的 | CNS以外の身体領域に病変を有する又は疑われる成人患者における、アムベルビスト(0.04mmol Gd/kg)の既承認mGBCA(0.1mmol Gd/kg;対照薬は試験方法を参照)に対する非劣性を検証する。 |
|---|---|
| 試験デザイン | 多施設共同、無作為化、二重盲検、クロスオーバー、16ヵ国(アジア、欧州、北米、南米)75施設 |
| 対象 | CNS以外の身体領域に病変を有する又は疑われる成人患者 |
| 例数(解析時) | 拡大FAS:379例※1、SAF:405例 〔うち日本人48例(アムベルビスト投与:48例、mGBCA投与:48例)〕 |
| 試験方法 | 各被験者をアムベルビスト(0.04mmol Gd/kg)又はmGBCA(ガドブトロール、ガドテル酸メグルミン又はガドテリドール:各0.1mmol Gd/kg)のいずれかに1:1の割合で無作為割付けし、2つの投与期にアムベルビスト又はmGBCAをクロスオーバーで単回静脈内投与した。1回目と2回目の造影MRI検査の間には3~14日間の休薬期間を設けた。各造影剤の投与前後にMRIを撮像し、非造影画像及び造影画像を取得した。得られた画像を盲検化した状態で独立した3名の読影医及び治験責任(分担)医師により評価した。評価は、MRI検査来院日(投与前から投与後6~8時間)に行った。 
|
| 主要評価項目 | 段階的スコアによる3つの描出パラメータ(造影効果、辺縁明瞭度、内部構造)[アムベルビスト組合せ※4のmGBCA組合せ※4に対する非劣性](検証的解析項目) ![段階的スコアによる3つの描出パラメータ(造影効果、辺縁明瞭度、内部構造)[アムベルビスト組合せ※4のmGBCA組合せ※4に対する非劣性]](/sites/g/files/vrxlpx8716/files/2026-03/products-ambelvist-clinical-trial_img-02.png)
|
| 主な 副次評価項目 | 病変検出能の感度及び特異度[アムベルビスト組合せ※4のmGBCA組合せ※4に対する非劣性] |
| 副次評価項目 | 段階的スコアによる3つの描出パラメータ(造影効果、辺縁明瞭度、内部構造)[アムベルビスト組合せ※4の非造影画像に対する優越性] など |
| 安全性評価項目 | 有害事象、理学的検査(視診、触診及び聴診)、バイタルサイン、臨床検査 |
| 解析計画 |
|
OBR(Other body regions):CNS以外の身体領域
CNS(Central nervous system):中枢神経系
mGBCA(Macrocyclic gadolinium-based contrast agent):環状型Gd造影剤
cSoT(Composite standard of truth):複合的な真の基準
TEAE(Treatment-emergent adverse event):治験薬投与下で発現した有害事象
◆
拡大FAS(Full analysis set):拡大した最大の解析対象集団(「盲検読影に適した造影MRI/MRA画像セットがある」「アムベルビスト組合せ及びmGBCA組合せの両方が評価可能である」の両方を満たすすべての無作為割付けされた被験者)
◆
SAF(Safety analysis set):安全性解析対象集団(アムベルビスト又はmGBCAを投与されたすべての無作為割付けされた被験者)
※ 1
拡大FASの379例中、読影医の評価が実施されたのは378例
※ 2
標的臓器の造影MRI検査の照会のために施設の標準治療方針に従って撮像した。
※ 3
施設の標準治療方針に従い、投与期1・2を通じて可能な限り同一条件(タイミング)で撮像した〔心臓MRIには2D/D-反転回復(IR)又は位相補正IR T1強調画像による遅延ガドリニウム造影(LGE)画像を使用した〕。
※ 4
アムベルビスト組合せ:アムベルビスト(0.04mmol Gd/kg)投与前後の組合せ画像、mGBCA組合せ:mGBCA(0.1mmol Gd/kg)投与前後の組合せ画像
※ 5
安全性の結果では、治験薬と関連のあるTEAEを「副作用」と表記した。
段階的スコアによる3つの描出パラメータ(造影効果、辺縁明瞭度、内部構造)
[アムベルビスト組合せのmGBCA組合せに対する非劣性]【主要評価項目(検証的解析結果)】
3つの描出パラメータにおけるアムベルビスト組合せとmGBCA組合せのスコアの差(最小二乗平均値)は、造影効果で0.06~0.03、辺縁明瞭度で−0.06~0.02、内部構造で−0.05~−0.01でした。3名の読影医において、3つの描出パラメータはいずれもスコアの差の95%信頼区間の上限値が非劣性マージンである0.35を下回り、アムベルビスト組合せのmGBCA組合せに対する非劣性が検証されました。
アムベルビスト組合せ及びmGBCA組合せにおける3つの描出パラメータ(造影効果、辺縁明瞭度、内部構造)のスコア※(拡大FAS)
表は横スクロールでご覧いただけます。
| アムベルビスト組合せ(N=378) | mGBCA組合せ(N=378) | ||
|---|---|---|---|
| 読影医1 | 造影効果 | 3.63±0.048 | 3.57±0.048 |
| 辺縁明瞭度 | 3.68±0.039 | 3.62±0.039 | |
| 内部構造 | 2.85±0.026 | 2.80±0.026 | |
| 読影医2 | 造影効果 | 3.11±0.048 | 3.13±0.048 |
| 辺縁明瞭度 | 3.63±0.039 | 3.65±0.039 | |
| 内部構造 | 2.75±0.026 | 2.74±0.026 | |
| 読影医3 | 造影効果 | 3.26±0.048 | 3.23±0.048 |
| 辺縁明瞭度 | 3.38±0.039 | 3.35±0.039 | |
| 内部構造 | 2.74±0.026 | 2.73±0.026 | |
最小二乗平均値±標準誤差
※
造影効果及び辺縁明瞭度は4段階、内部構造は3段階で評価した。3つの描出パラメータのスコアを線形混合効果モデルにより解析し、アムベルビスト組合せ及びmGBCA組合せの最小二乗平均値及び標準誤差を推定した。
アムベルビスト組合せ及びmGBCA組合せにおける3つの描出パラメータ(造影効果、辺縁明瞭度、内部構造)のスコアの差(拡大FAS)
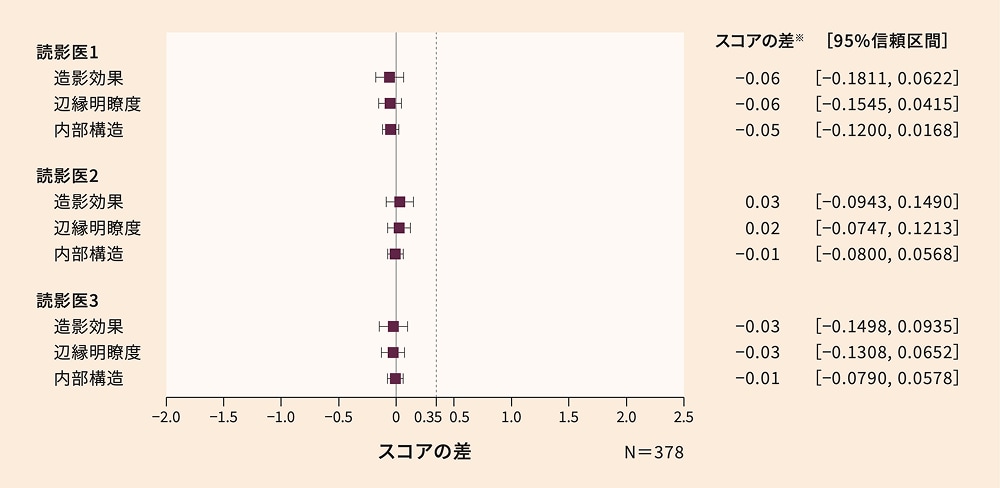
※
mGBCA組合せーアムベルビスト組合せ。3つの描出パラメータのスコアを線形混合効果モデルにより解析した。アムベルビスト組合せ及びmGBCA組合せの最小二乗平均値を推定し、更に各投与群間のスコアの差及びその95%信頼区間を推定した。3名の読影医のうち同じ2名の評価において、アムベルビスト組合せとmGBCA組合せのスコアの差の95%信頼区間の上限値が非劣性マージンである0.35を下回る場合、アムベルビスト組合せのmGBCA組合せに対する非劣性が検証されるものとした。
病変検出能の感度及び特異度[アムベルビスト組合せのmGBCA組合せに対する非劣性]【主な副次評価項目】
アムベルビスト組合せとmGBCA組合せの感度の差の95%信頼区間の上限値は、読影医1で4.41%、読影医2で2.38%、読影医3で5.86%であり、いずれも非劣性マージンである0.1(10%)を下回り、アムベルビスト組合せのmGBCA組合せに対する非劣性が示されました。アムベルビスト組合せとmGBCA組合せの特異度の差の95%信頼区間の上限値は、読影医1で9.33%、読影医2で9.73%、読影医3で18.51%であり、3名の読影医のうち2名において、非劣性マージンである0.1(10%)を下回り、アムベルビスト組合せのmGBCA組合せに対する非劣性が示されました。
アムベルビスト組合せ及びmGBCA組合せにおける病変検出能の感度※1及び特異度※2(拡大FAS)
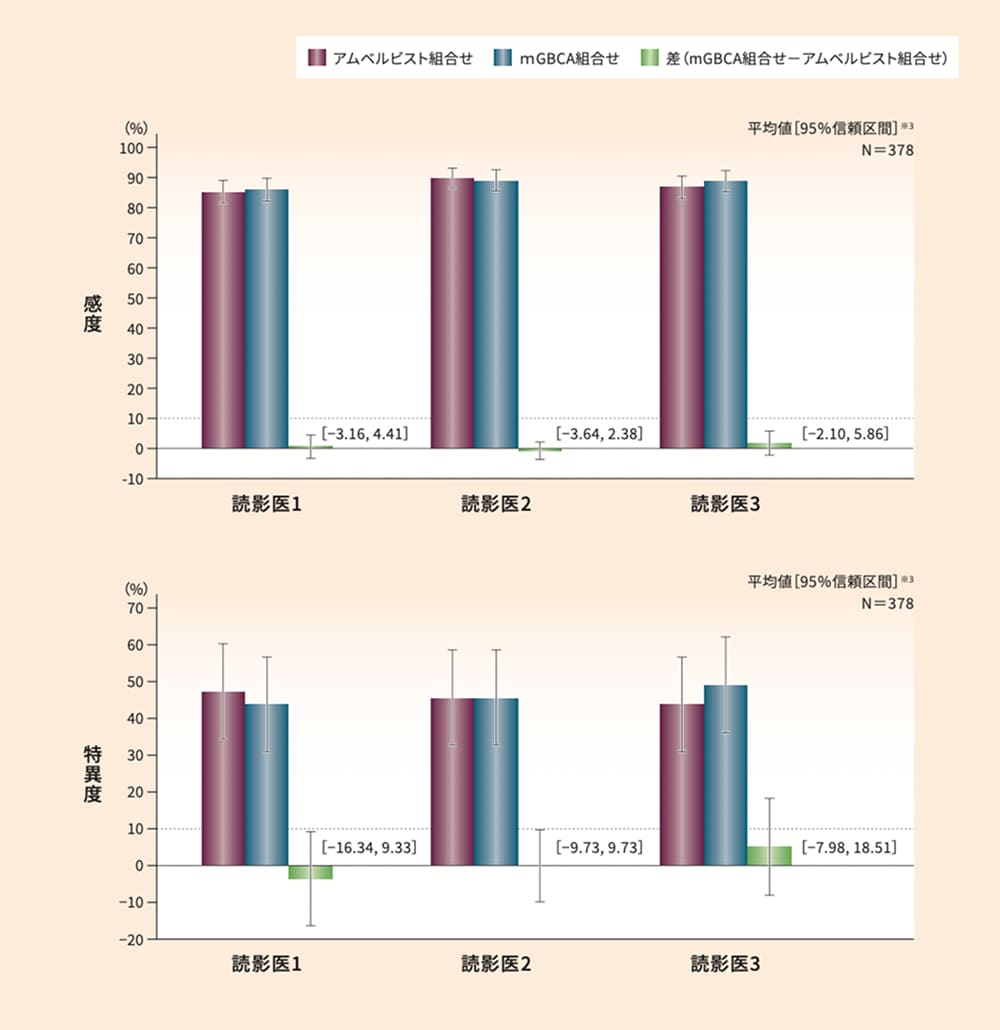
※ 1
読影医によって病変を有すると判定された被験者数をcSoTでの病変を有する被験者の総数で割った値として算出した。
※ 2
読影医によって病変がないと判定された被験者数をcSoTでの病変がない被験者の総数で割った値として算出した。
※ 3
読影医ごとに割合の差についてMcNemar検定に基づく95%信頼区間を算出した。3名の読影医のうち同じ2名の評価において、その上限値が非劣性マージンである0.1(10%)を下回る場合、アムベルビスト組合せのmGBCA組合せに対する非劣性が示されるものとした。
段階的スコアによる3つの描出パラメータ(造影効果、辺縁明瞭度、内部構造)[アムベルビスト組合せの非造影画像に対する優越性]【副次評価項目】
3名の読影医において、3つの描出パラメータのスコアの差(最小二乗平均値)※1は0.90~2.70であり、いずれも統計学的に有意であったため〔p<0.0001線形混合効果モデル、名目上のp値)〕、アムベルビスト組合せの非造影画像に対する優越性が示されました※2。
※1
アムベルビスト組合せ-非造影画像。造影効果及び辺縁明瞭度は4段階、内部構造は3段階で評価した。3つの描出パラメータのスコアを線形混合効果モデルにより解析した。アムベルビスト組合せ及び非造影画像の最小二乗平均値を推定し、更に各投与群間のスコアの差及びその95%信頼区間並びに標準誤差を推定した。
※ 2
3名の読影医のうち同じ2名の評価において、アムベルビスト組合せと非造影画像のスコアの差が0より大きく、統計学的に有意(片側有意水準:0.025)であった場合、アムベルビスト組合せの非造影画像に対する優越性が示されるものとした。
アムベルビスト組合せ及び非造影画像における3つの描出パラメータ(造影効果、辺縁明瞭度、内部構造)のスコアの差(拡大FAS)
表は横スクロールでご覧いただけます。
| スコアの差 | |||
|---|---|---|---|
| 読影医1(N=378) | 読影医2(N=378) | 読影医3(N=378) | |
| 造影効果 | 2.70±0.05 | 2.12±0.05 | 2.35±0.05 |
| 辺縁明瞭度 | 2.46±0.05 | 1.08±0.05 | 1.86±0.05 |
| 内部構造 | 1.70±0.03 | 0.90±0.03 | 1.67±0.03 |
最小二乗平均値±標準誤差


